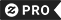Toque/clique na imagem para ver mais RealViewsTM
2,15 €
por cartão postal
Cartão Postal Mesa periódica dos elementos
Quantidade:
Tipo de papel
Fosco
-0,20 €
Atribuição
Sobre Postcards
Feito por
Sobre Esse Design
Cartão Postal Mesa periódica dos elementos
Em 1789, Antoine Lavoisier publicou uma lista de 33 elementos químicos. Embora Lavoisier tenha agrupado os elementos em gases, metais, não metais e terras, os químicos passaram o século seguinte buscando um esquema de classificação mais preciso. Em 1829, Johann Wolfgang Döbereiner observou que muitos dos elementos poderiam ser agrupados em tríades (grupos de três) com base em suas propriedades químicas. O lítio, o sódio e o potássio, por exemplo, foram agrupados como metais leves e reativos. Döbereiner também observou que, quando ordenado por peso atômico, o segundo membro de cada tríade era aproximadamente a média da primeira e da terceira[3]. Isso ficou conhecido como Lei de Tríades. O químico alemão Leopold Gmelin trabalhou com esse sistema e, em 1843, identificou dez tríades, três grupos de quatro e um grupo de cinco. Jean Baptiste Dumas publicou trabalhos em 1857 descrevendo relações entre vários grupos de metais. Embora vários químicos tenham sido capazes de identificar as relações entre pequenos grupos de elementos, ainda não tinham de criar um sistema que abrangesse todos eles[3]. O químico alemão August Kekulé havia observado em 1858 que o carbono tem tendência a se ligar a outros elementos numa proporção de um a quatro. O metano, por exemplo, tem um átomo de carbono e quatro átomos de hidrogênio. Este conceito acabou por se tornar conhecido como valência. Em 1864, o colega químico alemão Julius Lothar Meyer publicou uma mesa dos 49 elementos conhecidos arranjados por valência. A mesa revelou que elementos com propriedades semelhantes partilhavam frequentemente o mesmo valor[4]. O químico inglês John Newlands publicou uma série de artigos em 1864 e 1865 que descreviam sua tentativa de classificar os elementos: Quando listados por ordem de aumento do peso atômico, propriedades físicas e químicas semelhantes se repetiram em intervalos de oito anos, que ele comparou com as oitavas da música[5][6] Esta lei das oitavas, porém, foi ridicularizada pelos seus contemporâneos[7]. Retrato de Dmitri MendeleevO professor de química russo Dmitri Ivanovich Mendeleev e Julius Lothar Meyer publicaram independentemente suas mesas periódicas em 1869 e 1870, respectivamente. Ambos construíram as suas mesas de forma semelhante: ao listar os elementos numa linha ou coluna por ordem de peso atômico e ao iniciar uma nova linha ou coluna quando as características dos elementos começaram a repetir-se[8]. O sucesso da mesa de Mendeleev resultou de duas decisões que ele tomou: a primeira era deixar lacunas na mesa quando parecia que o elemento correspondente ainda não tinha sido descoberto[9]. Mendeleev não foi o primeiro químico a fazê-lo, mas foi um passo mais longe ao utilizar as tendências da sua mesa periódica para prever as propriedades desses elementos em falta, como o gálio e o germânio[10]. A segunda decisão foi ignorar ocasionalmente a ordem sugerida pelos pesos atômicos e trocar elementos adjacentes, como cobalto e níquel, para melhor classificá-los em famílias químicas. Com o desenvolvimento das teorias da estrutura atômica, tornou-se evidente que Mendeleev tinha listado inadvertidamente os elementos por ordem de aumentar o número atômico[11]. Com o desenvolvimento de teorias mecânicas quânticas modernas de configurações de elétrons dentro dos átomos, tornou-se evidente que cada fileira (ou período) na mesa correspondia ao preenchimento de uma casca quântica de elétrons. Na mesa original de Mendeleev, cada período tinha o mesmo comprimento. No entanto, dado que os átomos maiores possuem mais sub-cascas de eletrões, as mesas modernas têm vindo progressivamente a prolongar-se por períodos mais longos na mesa[12]. Nos anos seguintes a Mendeleev publicou sua mesa periódica, as lacunas que deixou foram preenchidas à medida que os químicos descobriam mais elementos químicos. O último elemento natural a descobrir foi o Francium (referido por Mendeleev como eka-césio) em 1939[13]. A mesa periódica também cresceu com a adição de elementos sintéticos e transurânicos. O primeiro elemento transurânico a ser descoberto foi o neptunium, formado pelo bombardeio de urânio com nêutrons em um cíclotron em 1939.
Tradução Automática
Comentários de clientes
5.0 de 5 estrelas3 Total de Comentários
3 Avaliações
Avaliações de produtos similares
5 de 5 estrelas
Por 18 de fevereiro de 2022 • Compra segura
Cartão Postal, Tamanho: Cartão postal padrão, Papel: Fosco , Envelopes: Nenhum
Programa de revisão da Zazzle
Overall satisfied with the product quality and time delivery. They forgot to send me the envelope but customer support promptly solved the problem. Will definitely buy again from Zazzle. Printing quality good (colors and semi-gloss finish came out as expected).
5 de 5 estrelas
Por 5 de junho de 2019 • Compra segura
Cartão Postal, Tamanho: Cartão postal padrão, Papel: Fosco , Envelopes: Nenhum
Programa de revisão da Zazzle
Veio exactamente como esperava e vou gostar muito de oferecer como lembrança de viagem a um familiar. A qualidade da impressão é incrível!
5 de 5 estrelas
Por 25 de novembro de 2016 • Compra segura
Cartão Postal, Tamanho: Cartão postal padrão, Papel: Fosco , Envelopes: Nenhum
Programa de revisão da Zazzle
Os postais chegaram fora de tempo, mas o produto é de excelente qualidade: boa impressão, cartão duro. Foi uma surpresa a qualidade. Muito bem! A impressão é de muito boa qualidade e exactamente o que pedi.
Tags
Outras Informações
ID de produto: 239531415535186043
Fabricado em 23/08/2009, 17:40
G
Itens visualizados recentemente